Interfaz ganado-fauna: enfermedades compartidas, factores de riesgo y control

La mayoría de las enfermedades infecciosas tienen como origen patógenos capaces de infectar a más de una especie animal, por lo que la dinámica epidemiológica de estos microorganismos se centrará en una comunidad multi-hospedador y, muchas veces, no muy restringida.
Este es el caso de un gran número de enfermedades que afectan el ganado vacuno en extensivo.
Así pues, este ganado vive en un hábitat caracterizado por una compleja red de contactos multiespecie, al aire libre, en grandes planicies y dehesas del ecosistema mediterráneo, dónde se produce el intercambio de recursos, pero también de patógenos infecciosos y vectores.
La preocupación por la existencia de un estrecho contacto entre el ganado en extensivo y la fauna silvestre existe desde hace muchas décadas, agravada en los últimos años debido al comprobado riesgo que representa la fauna silvestre para la sanidad del ganado y las consecuentes pérdidas económicas que conllevan las enfermedades asociadas.
En la Península Ibérica, especialmente en el ambiente mediterráneo, se estudian muchas patologías en el contexto de la interfaz ganado-fauna silvestre, siendo el caso más discutido y estudiado en la comunidad científica el de la tuberculosis (Richomme et al., 2013).
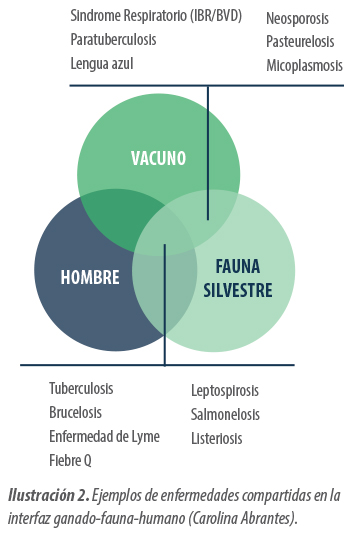
Además de la tuberculosis, se deben tener en cuenta más enfermedades compartidas entre el ganado y la fauna silvestre, por ejemplo:
- Paratuberculosis
- Síndrome respiratorio bovino (IBR/BVD)
- Lengua azul
El escenario se vuelve aún más complejo cuando hablamos de una interfaz ganado-fauna-humano, ya que muchas enfermedades del ganado doméstico compartidas con la fauna silvestre también son zoonóticas, demostrando ser un riesgo para los humanos, como en el caso de ganaderos o veterinarios (Gortázar et al., 2016).
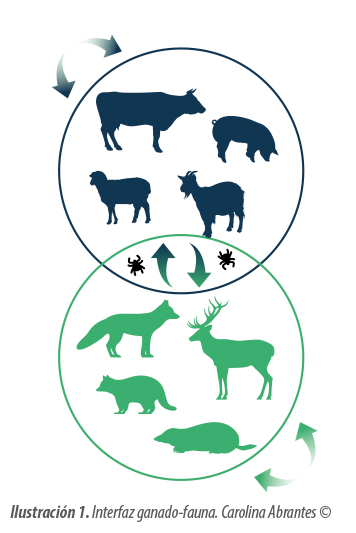
Para los ganaderos es muy importante comprender estos escenarios epidemiológicos multi-hospedador:
- Saber qué enfermedades circulan y su dinámica
- Cuáles son los principales factores de riesgo
- Especialmente, cómo prevenir estas enfermedades compartidas y/o controlarlas
ENFERMEDADES Y SU TRANSMISIÓN INTERESPECIE
En el ambiente mediterráneo, tanto en Portugal como en España, las dos enfermedades que más preocupación y pérdidas provocan, tanto a nivel de salud animal como de rentabilidad en la granja, son la tuberculosis y la brucelosis.
Ambas son enfermedades con planes de erradicación en curso y de fácil notificación y análisis de los brotes que puedan tener origen en la fauna silvestre.
En Portugal los datos apuntan a que más del 50% de los brotes de tuberculosis en vacuno en extensivo pueden tener como fuente primaria el contacto con la fauna silvestre cohabitante.
Cuando hablamos de fauna silvestre cohabitante, y enfocándonos en el centro-sur de Portugal y España, casi siempre están en nuestra mira las especies de caza mayor como el jabalí, el ciervo y/o el gamo.
Debido a la gran tradición cinegética en estas áreas mediterráneas es habitual que una misma explotación tenga dos finalidades diferentes: la ganadería extensiva y la caza.
Al no estar prohibido llevar a cabo ambas actividades en el mismo territorio, el ganadero y el gestor cinegético deben tener en cuenta:
- El riesgo sanitario al que están expuestos sus animales
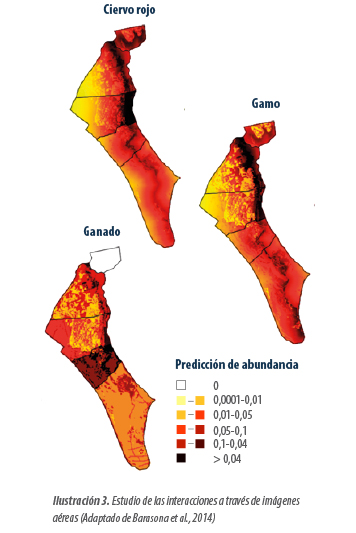
- Las consecuencias de las interacciones cotidianas en puntos de riesgo entre el ganado y la caza mayor (Cowie et al., 2014; Cowie et al., 2016; LaHue et al., 2016; Martínez-López et al., 2014).
El aumento de las interacciones multiespecie entre cohabitantes (ganado y fauna) se debe a una alteración previa de la estructura de la población silvestre consecuencia de alteraciones del hábitat:
- Superpoblación cinegética
- Área de circulación limitada
- Alimentación suplementaria disponible
- Uso de los mismos recursos que el vacuno en extensivo con nuevos patrones de pastoreo (Di Marco et al., 2012; Vicente et al., 2013)
Pero, aunque exista una convivencia y contacto diario entre los rumiantes domésticos y la fauna silvestre, la transmisión de enfermedades infecciosas compartidas dependerá de:
- Frecuencia y tipología de contacto
- Susceptibilidad de la especie para el patógeno circulante (Corner, 2006; Santos et al., 2009; Nugent et al., 2015)
CONTACTOS DIRECTOS
Se sabe que este tipo de interacción es más difícil que ocurra entre el ganado y la fauna silvestre.
Por su propia naturaleza, animales de diferentes especies se evitan y, generalmente, tienen sus picos de actividad diarios dispares (p. ej., el ganado vacuno es diurno y el jabalí es nocturno) (Kukielka et al., 2013).
Esporádicamente, se han observado contactos “próximos” en las zonas de riesgo, como los puntos de agua o de alimentación. Cuando esto ocurre puede producirse la transmisión de enfermedades por vía respiratoria, particularmente si hay alta densidad animal y el espacio es limitado (agregación espacial).
Algunos ejemplos de enfermedades transmisibles por vía respiratoria:
- Tuberculosis
- Síndrome Respiratorio (IBR/BVD)
- Micoplasmosis
- Pasteurelosis
CONTACTOS INDIRECTOS
Los contactos indirectos en la interfaz ganado-fauna son los que más posibilidad de transmisión posibilitan, ya que no necesitan estrictas condiciones espacio- temporales (Cowie et al., 2016).
La transmisión tiene lugar a través del suelo, alimento, pastos, agua o subproductos, o bien por contacto con animales enfermos excretores, a través de:
- Heces (vía fecal-oral)
- Orina
- Saliva
- Secreciones nasales o lacrimales
- Secreciones uterinas o de un aborto
Algunos ejemplos de enfermedades transmisibles por:
- Vía urinaria: leptospirosis y tuberculosis
- Vía fecal-oral: paratuberculosis, salmonelosis, campilobacteriosis, colibacilosis y clostridiosis
- Vía saliva, secreciones nasales o lacrimales: tuberculosis, pasteurelosis y micoplasmosis
- Vía secreciones uterinas o de aborto: brucelosis, neosporosis y clamidiosis
VECTORES
En una interfaz los vectores son también parte integrante del complejo multi-hospedador, y son varias las enfermedades transmitidas por vectores que pueden actuar en este sistema.
Culicoides, garrapatas y pulgas son algunos de los vectores biológicos capaces de transportar y transmitir diversos patógenos, siendo responsables de enfermedades como la Lengua Azul, Enfermedad de Lyme, Babesiosis, Thelaziosis, Fiebre Q o el Virus del Nilo Occidental.
Se pueden considerar factores de riesgo para enfermedades compartidas:
- Cualquier acción del ganadero y/o gestor cinegético o de fauna silvestre
- Condiciones ambientales
- Condiciones físicas de la explotación
Es decir, aquellos factores que faciliten la aparición de la enfermedad, su mantenimiento y la dispersión de esta en la comunidad multi-hospedador.
Así pues, para cuantificar el riesgo y analizar los factores presentes es necesario conocer las vías de trasmisión de las enfermedades y la persistencia y efectividad de estas durante el contacto en el interfaz ganado-fauna-humano.
¿CÓMO CONTROLAR LA DISPERSIÓN DE ESTAS ENFERMEDADES EN UNA EXPLOTACIÓN?
En un área de interfaz ganado-fauna, la eliminación/erradicación de una enfermedad compartida es muy difícil cuando:
- No se mantiene la integridad de los efectivos vacunos
- No se controlan y eliminan todos los reservorios
- No se controlan los factores de riesgo presentes en la explotación
Así, en un sistema multi-hospedador en áreas mediterráneas, el control sanitario es la medida con mejores resultados para minimizar los daños de la circulación de estas enfermedades (Gortázar et al., 2015).
Este control sanitario busca minimizar al máximo los efectos negativos en la sanidad animal, salud pública y en la economía de la presencia de la infección compartida por varios hospedadores cohabitantes pero, para establecer un plan de control sanitario contra determinada enfermedad, es necesario hacer un diagnóstico epidemiológico completo primero (Gortázar et al., 2011).
LOS 4 PASOS DEL DIAGNÓSTICO EPIDEMIOLÓGICO





 Latinoamérica
Latinoamérica
 Europa
Europa