Rumex: Valor añadido frente a la medicación contra coccidios

La aparición de los medicamentos antimicrobianos revolucionó la Medicina Humana y Veterinaria del Siglo XX, aportando tratamientos efectivos para las enfermedades causadas por microorganismos patógenos.

Desgraciadamente, estos microorganismos tienen la habilidad de evolucionar y desarrollar cepas resistentes a los antimicrobianos, dificultando cada vez más el tratamiento de las infecciones.
Esto ocurre cuando los microorganismos mutan o intercambian genes de resistencia y la utilización continua de los medicamentos antimicrobianos acelera el desarrollo de estas cepas resistentes.

| Hoy en día, la prioridad es salvaguardar la eficacia de estos medicamentos antimicrobianos, indispensables para tratar enfermedades en Medicina Humana. |
| La utilización de antimicrobianos en los animales de abasto puede favorecer la aparición de bacterias resistentes que pueden extenderse a las personas, tanto por contacto directo como a través de los alimentos |

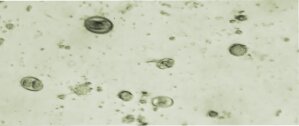
La coccidiosis es una enfermedad intestinal causada por parásitos unicelulares (protozoos).
Una vez que aparece la sintomatología en los animales, la enfermedad ya ha tenido un gran impacto negativo en su productividad. Por ello, utilizar medidas preventivas ha sido una práctica común en el sector ganadero.
COCCIDIOSTATOS
Tradicionalmente, la prevención se ha basado en el uso de coccidiostatos y coccidicidas, medicamentos/aditivos (rumiantes/ monogástricos) utilizados para prevenir la coccidiosis mediante la inhibición del crecimiento o provocando la muerte de los coccidios.
En la literatura científica ya se han descrito resistencias a todos los coccidiostatos autorizados en Europa, tanto a los ionóforos, como a los químicos o no ionóforos. También se ha demostrado que existe resistencia cruzada entre varios coccidiostatos, es decir, el desarrollo de resistencia frente a uno de ellos, conlleva la resistencia a otro.
COCCIDIOSTATOS IONÓFOROS
Una de las principales diferencias entre coccidiostatos ionóforos y coccidiostatos químicos es que los primeros también tienen acción bacteriostática y bactericida. También se ha demostrado la existencia de cepas bacterianas resistentes a ellos e incluso la capacidad de las bacterias de tener resistencias cruzadas.
COCCIDIOSTATOS QUÍMICOS
Actualmente, existen diferentes tratamientos frente a coccidios para rumiantes de cebo, en su gran mayoría de síntesis química (no-ionóforos), que pueden ser de administración puntual o continuada, preventiva y/o curativa.
![]() El decoquinato es un ejemplo representativo de estos tratamientos, administrándose en forma de premezcla medicamentosa durante un mínimo de 28 días.
El decoquinato es un ejemplo representativo de estos tratamientos, administrándose en forma de premezcla medicamentosa durante un mínimo de 28 días.
Productos como el decoquinato han demostrado reducir la carga parasitaria de los animales y las consecuencias de la enfermedad. Sin embargo, se están registrando efectos desfavorables:



La mayoría de los fitoquímicos (hasta hoy unos 55.000 identificados) de interés nutricional y farmacológico se clasifican habitualmente en:




| Alguno de estos alcaloides con aplicación clínica destacable son: aconitina (antirreumático), atropina (antiespasmódico), Xefedrina (descongestionante), ergotamina (migrañas), hidrastina (trastornos gastrointestinales) y morfina (dolor). |
¡Hoy en día, ya se han aislado más de 20.000 alcaloides!
Ciertos alcaloides poseen propiedades antiprotozoarias muy destacadas, mostrando una efectividad frente a coccidios similar a los medicamentos utilizados habitualmente en producción animal.




El producto comercial RUMEX incorpora en su composición alcaloides y posee propiedades antiprotozoarias destacables frente a coccidios, como se muestra en los siguientes experimentos. |

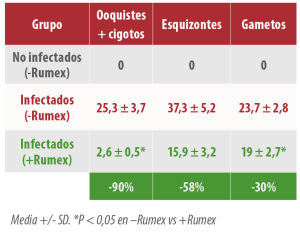
Tabla 1. Efecto de Rumex en las fases de desarrollo de E. papillata el día 5 post-infección (10 criptas intestinales) en ratones inoculados con ooquistes esporulados.

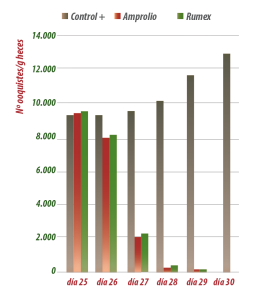
Gráfica 1. Efecto de Rumex y amprolio en la excreción de ooquistes de pollos desafiados con E. tenella (4.000 ooquistes/pollo) al día 20 de vida.
Gráfica 2. Efecto del Rumex y la combinación narasina + nicarbacina sobre la excreción de ooquistes en pollos desafiados con E. tenella (13.000 ooquistes/pollo).

En un experimento realizado con corderos de raza Rasa Aragonesa, se comparó la eficacia de decoquinato o Rumex frente a un control negativo durante el periodo de lactación.
A pesar de muestrear con hisopo rectal todos los animales, no se encontró presencia significativa de ooquistes en ningún grupo.
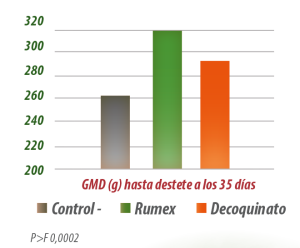
![]() Sin embargo, el crecimiento de los corderos fue mayor en los animales a los que se les administró decoquinato y mucho mayor en los que fueron suplementados con RUMEX en comparación con los animales control (Gráfica 3).
Sin embargo, el crecimiento de los corderos fue mayor en los animales a los que se les administró decoquinato y mucho mayor en los que fueron suplementados con RUMEX en comparación con los animales control (Gráfica 3). 
Gráfica 3. Ganancia Media Diaria (GMD) en corderos control o suplementados con decoquinato o Rumex.
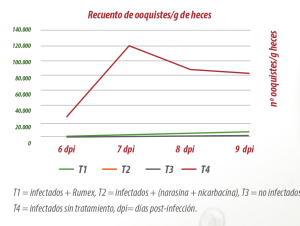
En otro experimento realizado con 48 terneros lactantes frisones de 55 kg PV, se administró RUMEX en la leche y se comparó la excreción de ooquistes frente a animales sin tratamiento. 
A pesar de que los animales ya excretaban ooquistes al comienzo del experimento, en el grupo RUMEX no se detectó excreción de ooquistes en los posteriores muestreos. En cambio, los terneros no tratados (control) continuaron excretando ooquistes durante todo el periodo experimental (Gráfica 4).
Este hecho también se reflejó como una mejora del crecimiento, consumo y conversión de los animales que consumieron Rumex en la leche (Tabla 2).
Gráfica 4. Excreción de ooquistes en terneros sin tratamiento o suplementados con Rumex.
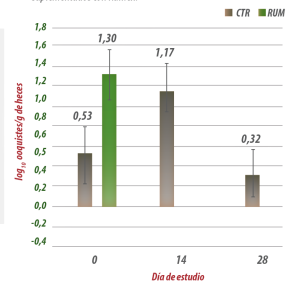
Tabla 2. Diferencias entre los valores de Ganancia Media Diaria (GMD), consumo de pienso e Índice de Conversión (IC) en terneros suplementados con Rumex en comparación con los terneros control.

En otro estudio realizado con terneras lactantes de recría, a pesar de que no se obtuvieron diferencias significativas en cuanto al análisis de la excreción de ooquistes en heces, se observó que la utilización de RUMEX:



| La aparición de microorganismos resistentes a los fitogénicos y, en particular, a RUMEX parece poco probable. |
 Para ilustrar este hecho, en un experimento se realizaron varios cultivos bacterianos con concentraciones sub-MIC (inferiores a las concentraciones mínimas inhibitorias) de RUMEX y 5 antibióticos a lo largo de 200 generaciones.
Para ilustrar este hecho, en un experimento se realizaron varios cultivos bacterianos con concentraciones sub-MIC (inferiores a las concentraciones mínimas inhibitorias) de RUMEX y 5 antibióticos a lo largo de 200 generaciones.
Mientras que se observó la aparición de bacterias resistentes a todos los antibióticos (E. coli) a las pocas generaciones, NINGUNA de las cepas mutó haciéndose resistente frente a RUMEX.
| La razón por la que RUMEX no genera resistencias puede deberse a su modo de acción, ya que actúa sobre funciones esenciales de la vida de las células como la replicación de ADN o la transcripción de ARN, alterando su actividad enzimática y dañando la estructura celular. |
![]() En consecuencia, si alguna mutación recayera en alguna de estas funciones básicas, ésta seguramente sería letal y las bacterias no serían viables.
En consecuencia, si alguna mutación recayera en alguna de estas funciones básicas, ésta seguramente sería letal y las bacterias no serían viables.
| CONCLUSIÓN |
|
RUMEX permite controlar de manera eficaz y económicamente competitiva el crecimiento de coccidios sin la necesidad de utilizar coccidiostatos ionóforos ni químicos.
En rumiantes en particular, a pesar de que a veces resulta complicado extraer conclusiones del recuento de ooquistes en heces, el hecho de que no aparezcan diarreas en los animales y que el crecimiento diario sea bueno, confirma de forma indirecta la eficacia de RUMEX en el control de coccidios. |





 Latinoamérica
Latinoamérica
 Europa
Europa
































